
近期,中科院合肥研究院强磁场中心王俊峰、周数研究团队在线粒体蛋白跨膜转运研究领域取得了突破性进展:利用液体核磁共振技术在国际上首次解析出酵母线粒体内膜Tim23通道蛋白与其底物肽段的复合物三维空间结构。相关研究成果以“Solution structure of the voltage-gated Tim23 channel in complex with a mitochondrial presequence peptide”为题发表在国际期刊Cell Research上。
线粒体拥有复杂而又精细的蛋白质转运系统来介导不同的细胞质前体蛋白转运至线粒体各区域。Tim23通道蛋白自身或在其他相关亚基帮助下,可以特异性识别细胞质前体蛋白并转运至线粒体基质内或者插入到线粒体内膜中。近年来,围绕该通道蛋白的功能研究取得了很大的进步,但是Tim23 通道蛋白的三维空间结构依然未知。
该项研究工作中解析了Tim23-pCoxIV复合物结构,其是目前利用液体核磁共振技术所解析的分子量最大的膜蛋白复合物之一,并且发现了一系列独特的空间结构特点。首先是Tim23蛋白N端膜外区域包含了一个特异性识别、结合前体蛋白的结构域。其次是Tim23通道蛋白的控制开关采用了双开关控制机制:第一重开关是由六个带电荷氨基酸残基构成的三对离子键,存在于内膜表面之上,起到电压感受器的作用;第二重开关是存在于通道顶端开口内的芳香族氨基酸侧链,起到空间位阻的作用。最后是通道的结合界面是依靠弱氢键维系,在前体蛋白进入通道以后,同时能够打破氢键,从而使通道解离为单体。基于体外电生理实验结果以及以上蛋白结构特点,研究人员提出了Tim23通道蛋白跨膜转运细胞质前体蛋白的分子机制模型。
该项研究获得国家自然科学基金、中科院人才项目基金和欧盟Horizon 2020项目基金的支持。核磁共振实验受到稳态强磁场实验装置和德国法兰克福大学核磁中心的支持。
文章链接:https://www.nature.com/articles/s41422-020-00452-y
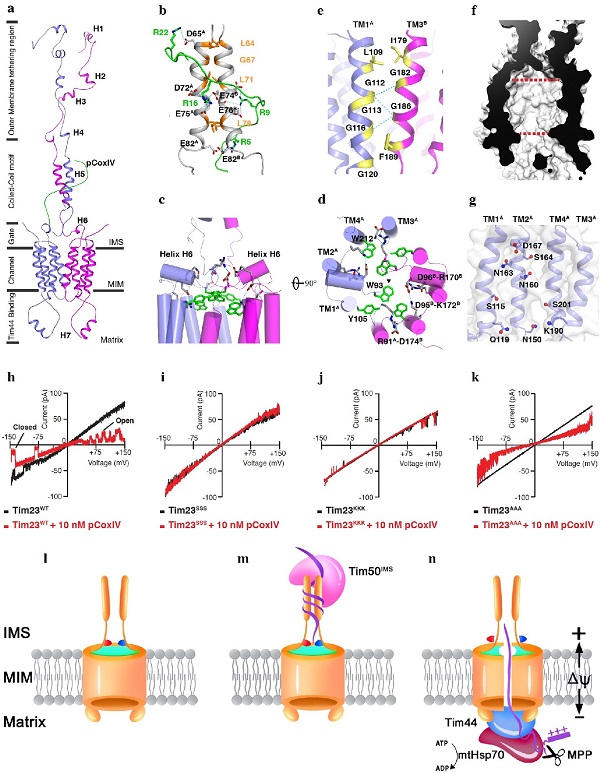 Tim23-pCoxIV复合物的溶液状态三维空间结构。
Tim23-pCoxIV复合物的溶液状态三维空间结构。
a.Tim23-pCoxIV复合物三级结构;b. Tim23蛋白N端识别底物的结合方式;c.通道分子开关1-电压感受器;d.通道分子开关2-多对芳香族氨基酸簇;e.Tim23蛋白二聚体结合界面;f.蛋白质转运通道纵向切面视图;g.蛋白通道内侧氨基酸分布; h,i,j,k.Tim23野生型及功能区域突变体的电生理分析; I,m,n.Tim23通道蛋白转运分子机制模型.